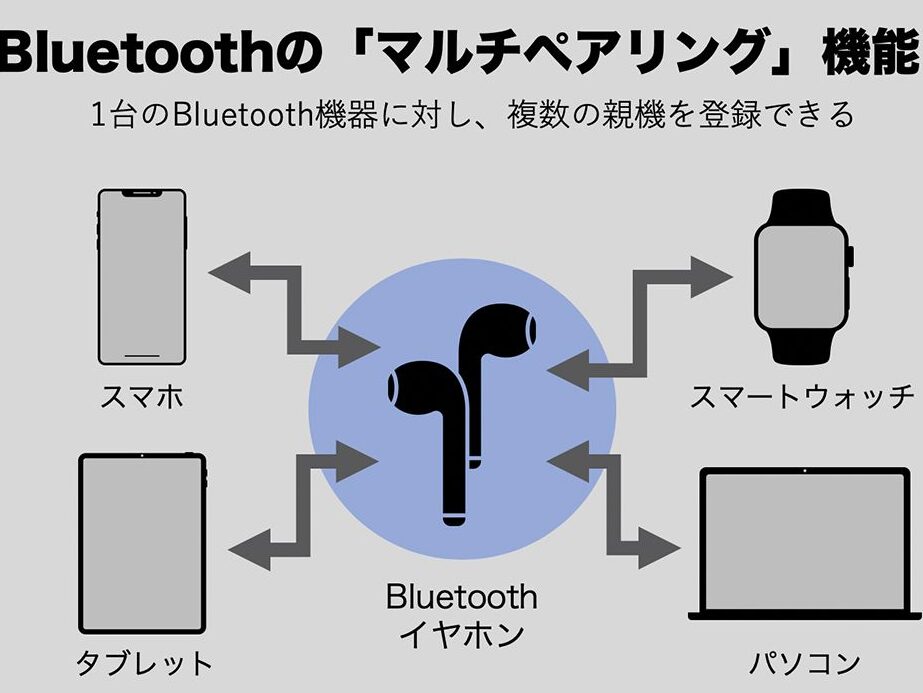
スマホのペアリングって何ですか?私たちの日常生活において、スマートフォンは欠かせない存在となっています。その中でも特に重要なのが、他のデバイスとのスムーズな接続を実現するペアリング機能です。この機能を理解することで、より便利で快適なデジタルライフを送ることができます。
この記事では、スマホのペアリングって何ですか?という疑問にお答えし、その仕組みや具体的な使い方について詳しく解説します。BluetoothやWi-Fiなどの技術を活用してどのようにデバイス同士がつながるのか知ることで、新しい可能性が広がります。さあ、一緒にこの魅力的なテーマについて探求してみましょう!あなたも新たな発見を楽しみにしているはずです。
スマホのペアリングって何ですか?その基本的な仕組み
私たちが探求する「スプラのスプライシング」とは、遺伝子を編集する際に重要な技術です。このプロセスは、特定の遺伝子からイントロン(不要な部分)を除去し、エクソン(必要な部分)を結合させることで成り立っています。これにより、正確で機能的なメッセンジャーRNA(mRNA)が生成され、その後、タンパク質合成が行われます。
スプライシングにはいくつかの基本的な概念があります。まず、エクソンとイントロンの違いを理解することが重要です。エクソンはタンパク質コーディング領域であり、一方イントロンはタンパク質には関与しない非コーディング領域です。この区別が正しいスプライシングに不可欠です。
次に、このプロセスを実現するために必要な酵素や複合体について考えましょう。以下は主な要素です:
- スプライソソーム:エクソンとイントロンの切断・接続を行う大きな酵素複合体。
- snRNA(小核RNA):スプライソソームの一部として機能し、RNA構造や相互作用を調整します。
- 補助因子:他のタンパク質やRNA分子もこの過程でサポート役として働きます。
また、この過程には様々な種類があります。例えば、
- 選択的スプライシング:同じ遺伝子から異なるmRNAが生成され、多様性を生み出します。
- 恒常的スプライシング:特定の条件下で一貫して行われるプロセス。
これらの知識は、新たな治療法やバイオテクノロジーへの応用につながる可能性があります。我々はこの分野で進展し続けており、その影響力は今後さらに広がっていくでしょう。
ペアリングの手順と必要な準?
私たちが考えるに、スプライシングの手段と必要な要素は非常に密接に関連しています。具体的には、スプライシングとはRNA前駆体から不要な部分を取り除き、有用な部分を結合する過程です。このプロセスは、細胞内での遺伝子発現調節やタンパク質合成において重要な役割を果たします。また、このプロセスが適切に行われることで、正確なmRNAが生成され、その後の翻訳過程が円滑に進むことにつながります。
- エキソン:これは遺伝子の中で実際に有用な情報を持つ部分です。エキソンは最終的に成熟したmRNAになる際には残されます。
- イントロン:この部分は通常、不必要とされており、スプライシングの過程で除去されます。イントロンが存在すると、RNAの安定性や機能にも影響を与える可能性があります。
- リボザイム:特定の条件下で自身を切断する能力を持つRNA分子です。これらもスプライシング過程には関与しており、自動的な切断によって効率的な処理が促進されます。
また、私たちが知っているように、このプロセスにはいくつかの異なるメカニズムがあります。それぞれについて理解することで、より深い洞察を得ることができるでしょう。
- 酵素依存型スプライシング: 特定の酵素(スプライソソーム)が関与し、高度な精度でイントロンを除去します。
- 自己触媒型スプライシング: 一部のRNA分子自身が反応し、自らイントロンを除去します。このメカニズムではリボザイムとして知られるものも利用されています。
これら多様なメカニズムのおかげで、生物は効率よく複雑な遺伝情報を管理し、それぞれ適応したタンパク質合成へと繋げることができます。我々としては、このような仕組みへの理解こそ、新しい治療法や技術開発につながる鍵だと考えています。
ペアリングができるデバイスの種類
私たちは、スプライシングがどのように行われるかを理解することが重要であると考えています。これは、RNA前駆体から成熟mRNAへの変換プロセスにおいて不可欠なステップです。この過程では、イントロンと呼ばれる不要な部分が切り取られ、エクソンと呼ばれる情報を持つ部分が結合されます。これにより、タンパク質合成のための正確なメッセージが生成されます。
- エクソン:これらは遺伝情報を含むRNAの部分であり、最終的に翻訳されてタンパク質になります。
- イントロン:これらは不要な領域であり、スプライシングによって除去されます。この工程が正しく行われないと、不完全なmRNAが生成される可能性があります。
- スプライシング因子:特定のタンパク質や小さなRNA分子(snRNA)がこのプロセスを助けます。彼らはイントロンを認識し、それを取り除くための複雑な機械構造を形成します。
また、私たち自身もこのプロセスにおいていくつかの要因によって影響を受けることがあります。例えば、細胞内環境や外部ストレス要因などです。それぞれの条件下でどのようにスプライシングが変化するかについても知識を深めていく必要があります。
| 要因 | 影響内容 |
|---|---|
| 温度変化 | 適切温度範囲外では効率的なスプライシングが妨げられる場合があります。 |
| 栄養状態 | 栄養素不足は細胞機能全般に影響し、その結果としてmRNA生成にも支障をきたす可能性があります。 |
| ストレス応答 | 細胞ストレス時には特定の遺伝子発現パターンが促進され、それによってスプライシング選択肢も変わります。 |
This understanding of splicing and its regulatory mechanisms is crucial for our further research. By focusing on these details, we can enhance our grasp of gene expression and its implications in various biological contexts.
スマホを使った便利な活用法
私たちが注目すべきは、スプライシングの過程でRNAのさまざまな利用法です。このプロセスは、生物学的機能を持つmRNAを生成するために不可欠です。特に、異なる条件下で細胞内でどのように調整されるかについて理解を深めることが重要です。以下では、スプライシングによって生じるmRNAのバリエーションとその生理的意義について詳しく説明します。
スプライシングによるmRNAの多様性
スプライシングは、遺伝子から転写された前駆体mRNA(pre-mRNA)からイントロンを除去し、エクソンを連結することで機能的なmRNAへと変換する過程です。このプロセスにはいくつかの重要なステップがあります:
- イントロン除去: 不要な部分であるイントロンが取り除かれます。
- エクソン連結: 残ったエクソンが順番に接続されていきます。
- ポリA尾部追加: mRNA末端にポリA尾部が付加されることで安定性が増します。
このようにして生成されたmRNAは、多様なタンパク質同位体(アイソフォーム)をコードする可能性があります。これにより、生物は同一の遺伝子から異なる機能を持つタンパク質を作り出すことができ、その結果として細胞や組織特異的な機能が発現します。
スプライシング調節因子
スプライシングには多くの調節因子が関与しており、それぞれ異なるメカニズムで働きます。以下は主な調節因子です:
- SRタンパク質: エクソンへの選択的結合によって、スプライシング活性化に寄与します。
- hnRNPタンパク質: 主にイントロンやエクソンへの結合を通じて、抑制作用及び活性化作用があります。
- miRNA: 特定のターゲットmRNAとの相互作用によって翻訳抑制や分解促進なども行います。
これらの因子は、外部環境や細胞内条件によって変動し、それぞれ異なる影響を及ぼすため、私たちはそれらの相互作用について詳細に研究していく必要があります。
| 調節因子 | 役割 |
|---|---|
| SRタンパク質 | エクソン選択と活性化促進 |
| hnRNPタンパク質 | イントロン・エクソン間で複雑な役割 |
| miRNA | ターゲットmRNAとの相互作用による翻訳抑制 |
このような理解こそが、私たち自身の研究活動や医療応用につながります。スプライシングメカニズムとその調節因子について更なる知見を得ることで、新しい治療法開発へとつながる可能性があります。
トラブルシューティング:よくある問題と解決策
私たちは、核酸の合成における重要な役割を果たすmRNAの特性について理解を深め、その機能を最大限に活用するための戦略を検討しています。mRNAは遺伝子情報の伝達を担うだけでなく、細胞内での多くのプロセスにも関与しており、その調整メカニズムは生物学的研究や医療応用において非常に重要です。
mRNA分解経路
mRNAが細胞内でどのように分解されるかは、その安定性や持続時間に大きく影響します。以下は、主要なmRNA分解経路とその特徴です。
- デポリメラーゼ経路: mRNAが5’キャップ構造を失うことで始まり、ヌクレアーゼによって切断されます。
- エキソソーム経路: 細胞質内で複数の酵素からなるエキソソームによってmRNAが逐次的に分解されます。この過程では、主に3’末端から開始されます。
- 内部切断経路: 特定のシグナルや因子によって引き起こされる内部切断が行われることがあります。このメカニズムは特異的な条件下でのみ発現します。
これらの分解経路は、それぞれ異なる制御因子によって調節されています。また、環境要因や細胞ストレスもこれらの過程に影響を与えるため、私たちはその理解を深める必要があります。例えば、特定のmiRNAやタンパク質がこれらの過程に関与していることが知られており、この知識は新しい治療法開発への手助けとなります。
mRNA安定性と調節因子
mRNAの安定性にはさまざまな要因が作用し、それぞれ相互作用しながら全体的な発現量へ影響します。私たちが注目すべき主な調節因子には以下があります:
- キャッピングとポリアデニル化: mRNA 5’末端へのキャップ付加と3’末端へのポリアデニル化は、その安定性向上につながります。
- 翻訳後修飾: タンパク質合成後に行われる修飾も、間接的にもmRNA の寿命や活性へ影響します。
- BMP関連因子: 骨形成タンパク質(BMP)など特定タンパク質もmRNA の安定化及び翻訳促進として知られています。
このような知見から得られる情報群は、新しい治療法やバイオテクノロジー製品開発へとつながります。我々自身でも、この領域で今後さらに探究していく必要があります。それによって得られる新たな洞察こそが、生物医学研究・臨床応用へ向けて大いなる前進となるでしょう。
| Molecular Mechanism | Description |
|---|---|
| Error-prone pathways | Mediated by environmental stressors affecting mRNA stability. |
| Synthetic approaches | Using modified nucleotides to enhance stability and efficacy. |
| Targeting techniques | Leveraging miRNAs or proteins for controlled degradation. |
This exploration into the mechanisms governing mRNA dynamics not only enhances our understanding but also paves the way for innovative therapeutic strategies. We must remain vigilant in our research endeavors as we seek to unravel further complexities of genetic regulation in cellular contexts.